なぜ今「薬剤耐性菌(AMR)」が問題なのか
現在、世界各国で抗生物質が効かない細菌「薬剤耐性菌(AMR:Antimicrobial Resistance)」が増えていることが、大きな社会問題となっています。
薬剤耐性菌が増えると、これまでなら短期間の治療で治っていた感染症でも、治療が難しくなったり、重症化したりするリスクが高まります。
2050年には、薬剤耐性菌が年間1,000万人の死亡原因になる可能性があるという予測もあります。これは、がんによる死亡者数をも上回る規模とされ、人類の健康にとって非常に大きな脅威です。
抗生物質が十分に効かない時代が現実のものとなりつつあることから、薬剤耐性菌は世界中の研究者やメディアから強い関心を集めています。
そんな中で細菌に特異的に感染するウイルス「バクテリオファージ」を使った「ファージ療法」への注目度が高まりつつあります。この記事では「ファージ療法とは何か」「なぜ今注目されているのか」「現時点でどこまで研究が進んでいるのか」を分かりやすく解説します。
薬剤耐性菌が生まれるしくみ
薬剤耐性菌(AMR)は、抗生物質の使いすぎによって自然に増えてきた細菌です。
こうした状況では、抗生物質とは異なる仕組みの対策が必要とされており、その一つがファージ療法です。
薬剤耐性菌が生まれる3つの理由

抗生物質の使いすぎ・乱用
抗生物質は、細菌による感染症を治療するうえで欠かせない薬です。一方で、本来必要のない場面で抗生物質が使われると、薬剤耐性菌が生まれる大きな原因になります。
例えば、風邪の多くはウイルス感染によるものですが、ウイルスに対して抗生物質は効果がありません。それにもかかわらず、ウイルス性疾患に対して抗生物質が使われることがあり、こうした使用が繰り返されることで、細菌が抗生物質にさらされる機会が増えます。その結果、抗生物質の影響を受けにくい細菌だけが生き残り、耐性を獲得していくのです。
耐性菌の広がりやすい環境
薬剤耐性菌の問題は、人の医療現場だけで生じているわけではありません。抗生物質の使用量のうち、人に使われるのは全体の一部であり、家畜や養殖魚、農業分野などでも抗生物質が使用されてきました。
病院や畜産現場のように、抗生物質が繰り返し使われる環境では、耐性菌が生まれやすくなります。こうして生まれた耐性菌は環境を通じて広がる可能性があります。そのため、人・動物・環境を一体として考える視点が重要です。
進化と自然選択による耐性獲得のメカニズム
細菌が薬剤耐性を獲得するのは、特別なことではなく、生き残るための自然な進化の結果です。
抗生物質が使われる環境では、感受性のある細菌は死滅し、偶然耐性を持っていた細菌だけが生き残ります。そして生き残った細菌が増殖することで、抗生物質が効かない細菌が集団の中で主流になっていくのです。
こうした状況の中で、抗生物質に代わる新しいアプローチとして注目されているのが“ファージ療法”です。
ファージとは何か?なぜ医療に使える可能性があるのか?
バクテリオファージの定義
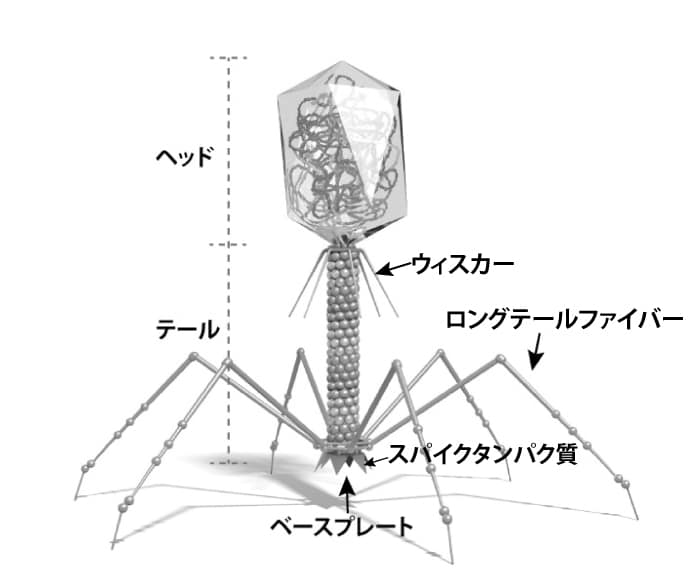
ファージとは、正式には「バクテリオファージ」と呼ばれ、細菌に感染するウイルスの総称です。研究や一般向けの記事では、簡潔に「ファージ」と呼ばれています。
細菌だけを狙って感染・増殖する特徴
ファージの大きな特徴の一つは、感染する相手を非常に厳密に見分ける点にあります。
それぞれのファージは、特定の細菌だけをターゲット(宿主)としており、狙った細菌以外には感染しません。この高い感染の特異性は、抗生物質のように広範囲の菌を一律に攻撃するのとは大きく異なります。
細菌を溶かして退治する「溶菌」の仕組み
ファージは、細菌の表面にある目印を認識して結合し、自分の遺伝子だけを細菌の中に注入します。
その後、細菌の仕組みを利用して子ファージを増殖させ、最終的に細菌を内側から壊して、増えた子ファージを放出します。この過程を「溶菌」と呼びます。
製品や医療応用で主に利用されているのは、この溶菌を起こす「溶菌性ファージ」であり、細菌を確実に破壊する働きを持つタイプです。
人体には無害で自然界に広く存在する
「ウイルス」と聞くと危険な印象を持たれがちですが、ファージは人の細胞には感染しません。
ファージは自然界に広く存在しており、土壌や水中だけでなく、人の腸や皮膚など体内にも数多く存在していることが知られています。
なぜ「ファージ療法」が再注目されているのか
抗生物質が効かない耐性菌にも効果が期待される
近年、世界各国で抗生物質が効かない薬剤耐性菌(AMR)が増加し、従来の治療が通用しない感染症が問題となっています。こうした状況の中で、抗生物質とは異なる仕組みで細菌に作用するファージ療法が、耐性菌対策の新たな選択肢として注目されています。
ファージは、抗生物質に耐性を獲得した細菌であっても、感染・増殖し、溶菌することが可能です。この点が、耐性菌問題が深刻化する現在において、再評価されている理由の一つです。
ロシア・ジョージアなどでの長年の臨床利用歴
ファージ療法は決して新しい概念ではなく、ロシアやジョージアなどでは、抗生物質が普及する以前から治療に用いられてきた歴史があります。
欧米・日本での研究加速
抗生物質耐性菌の拡大を受けて、近年は欧米や日本でもファージ療法に関する研究が急速に進められています。
海外では、治療選択肢が尽きた重症感染症に対する「救済的治療」としてファージが使用された事例が報告され、これをきっかけに研究や制度整備が進んでいます。
日本においても、研究者によって、ファージの基礎研究から医療応用、社会実装を見据えた議論が進められており、薬剤耐性菌対策の一環として注目が高まっています。
薬剤耐性菌とファージ療法の相性
“抗生物質 vs 耐性菌” の限界
様々な抗生物質を使えば、各抗生物質に対し耐性を持つ細菌が選択的に生き残るため、「効く薬が徐々に失われていく」状況が生まれます。
耐性菌問題が深刻化しているにもかかわらず、製薬会社は新しい抗生物質の開発に積極的とは言えないのが現状です。
医薬品の研究開発には一般に10年以上の期間が必要であり、成功確率も年々低下しています。
さらに抗菌薬は、抗がん剤などと比べて投与期間が短く、薬価も高く設定しにくいという特徴があります。そのため、新規抗生物質を開発しても、十分な収益が見込めず、むしろ赤字になる可能性が高いと指摘されています。
加えて、新規抗生物質が上市されたとしても、ほどなく耐性菌が出現してしまう可能性が高いことも、製薬企業の開発意欲を削ぐ要因となっています。
このように、抗生物質と耐性菌の関係は、「新規抗生物質の開発 → 使用 → 耐性菌の出現 → 殺菌効果の低下」という循環に陥りやすく、企業努力だけでは解決しにくい構造的限界を抱えているのです。
“ファージ療法 vs 耐性菌” の強み
ファージの作用機序は抗生物質の作用機序と異なるため、抗生物質耐性菌を制御することができます。
こうした性質からファージ療法は、抗生物質が効かなくなった耐性菌に対しても理論的には有効性が期待される療法として位置づけられています。
ファージは細菌が耐性を獲得しても追随できる(共進化)
細菌がファージに対して耐性を獲得する可能性はありますが、ファージ自身も進化する存在です。自然界では、細菌とファージは長い時間をかけて互いに影響を与え合いながら共存・共進化してきました。この点は、単一の化学物質である抗生物質とは異なる、動的な対抗関係といえます。
抗生物質と併用することで相乗効果が期待されるケースも
近年の研究では、ファージと抗生物質を併用することで、治療効果が高まる可能性がある「ファージ・抗生物質相乗効果(PAS: Phage Antibiotic Synergy)」が報告されています。
抗生物質が細菌の状態を変化させることで、ファージの感染や増殖が促進されるケースや、逆にファージが細菌に感染すると、細菌の細胞壁が部分崩壊し、そこから抗菌薬が効率的に細胞内へ侵入するため抗生物質が効きやすくなる可能性が示唆されています。
世界・日本でのファージ療法研究の最新動向
欧米で進む臨床試験

欧米では、ファージ療法を「将来の感染症治療の選択肢」として位置づけ、臨床研究や臨床試験の枠組みの中で検証する動きが進んでいます。
欧米で採られている2つの臨床アプローチ
欧米におけるファージ療法の臨床利用は、大きく2つの形に分かれています。
1つ目は、通常の医薬品と同様に、治験(GCP:Good Clinical Practice)として実施される臨床試験型です。
この場合、複数のファージを混合した製剤(ファージカクテル)を用い、有効性や安全性を段階的に評価します。
米国を中心に、この「標準化された製剤」としてのファージ療法が、抗菌薬の代替・補完候補として検証されています。
2つ目が、ベルギーなどで見られる、抗生物質による標準治療が無効となった患者を対象とした個別化医療型の臨床利用です。
これは、患者から分離された原因菌に適合するファージを選定・調製し、医師主導で投与する形の臨床的使用であり、従来型の治験を経た医薬品とは異なる位置づけで行われています。
日本国内の動向
日本においても、ファージ療法に関する研究・開発は、大学や公的研究機関を中心に着実に進められています。
大学・研究機関による基礎研究の蓄積
日本ではこれまで、ファージの働きや細菌との関係を明らかにする基礎研究が中心的に行われてきました。
近年では、薬剤耐性菌問題への関心の高まりを背景に、ファージを感染症対策の一つの選択肢として捉える研究も増えています。
医学・薬学・獣医学・微生物学など、分野を横断した研究者同士の連携も進み、国内の研究成果を共有するための研究会や学術集会も活発に開催されています。
医療応用を見据えた研究拠点の形成
一部の大学では、ファージ療法を将来の医療技術として捉え、基礎研究から社会実装までを視野に入れた研究拠点が設けられています。
これらの拠点では、単に研究成果を論文として発表するだけでなく、制度や安全性、実用化の課題も含めた検討が行われています。
また、獣医学系の大学や研究機関では、動物医療や畜産分野での感染症対策としてファージ研究が進められており、こうした知見が人の医療に応用される可能性も期待されています。
企業による段階的な研究開発
日本企業におけるファージ関連の開発は、医薬品としてのファージ療法をいきなり目指すケースは多くありません。
その背景には、日本の薬機法(医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律)ではファージ療法を医療として運用するハードルが高いという現実があります。
そのため企業の多くは、
● 皮膚や口腔、腸内などの局所的な領域
● 食品・環境分野での細菌コントロール
といった、比較的制度上の制約が少ない分野から研究・応用を進めています。
医療応用へ向けた課題
ファージ療法は、非常に有望なアプローチとして注目されていますが、医療として広く使われるためには、いくつもの現実的な課題を乗り越える必要があります。
既存の医薬品制度に当てはめにくい

ファージ療法は、従来の医薬品とは根本的に性質が異なるため、既存の医薬品承認制度にそのまま当てはめることが難しい治療法とされています。
一般的な医薬品制度は、
● 成分や構造が固定されている
● 製造工程が一定である
● 大量生産され、多くの患者に同一の製品が使われる
ことを前提に設計されています。
一方で、ファージは、細菌との相互作用の中で突然変異や性質の変化を起こしうる存在であり、培養や継代の過程で性状が変化する可能性があります。
規制の観点からは、
● 「どこまでを同一製品とみなすのか」
● 「性質が変化した場合、再評価が必要か」
● 「変異や進化をどう品質管理に組み込むのか」
といった問題が生じます。
これは、安全性への懸念というよりも、生きたウイルスを治療に用いるという特性を、既存制度が想定していないことに起因する課題といえます。
今後に向けた動きと可能性
標準化に向けた国際的議論
現在、欧米を中心に、ファージ療法をどのように評価し、どの基準で品質や安全性を担保するかについて、国際的な議論やガイドライン整備が進んでいます。
AIや合成生物学を活用した研究の進展

また近年では、AIや合成生物学の技術を活用し、ファージと細菌の関係をより正確に解析したり、設計・最適化する研究も進んでいます。
まとめ:薬剤耐性菌拡大の時代に期待される新しい希望

薬剤耐性菌(AMR)は、遠い未来の話ではなく、すでに私たちが直面している課題です。抗生物質が効かない感染症が増えるなかで、これまで当たり前だった治療が通用しなくなる可能性は、誰にとっても無関係ではありません。
そうした状況の中で注目されているのが、ファージ療法です。ファージ療法は、抗生物質を完全に置き換える「万能な治療法」ではありませんが、抗生物質に依存しすぎない医療を支える、新しい選択肢の一つとして研究が進められています。欧米を中心に、臨床研究や制度設計の試みが積み重ねられていることは、薬剤耐性菌対策における重要な前進といえます。
一方で、ファージ療法を社会実装するにあたり、規制の問題など解決すべき課題も少なくありません。
研究が進む今、ファージ療法は薬剤耐性菌拡大の時代における新しい希望の芽として、少しずつ形になりつつあります。確実な検証と議論を重ねながら、将来の医療にどのように生かされていくのかを見守っていくことが大切だといえるでしょう。
参考文献:
Japanese Society for Infectious Diseases. “Guidelines for Personalized Phage Therapy.” (2023).
EU-JAMRAI. “Sustainable implementation of phage therapy across the EU – Meeting Report.” (2024).






